Células madre mesenquimales: aspectos relevantes y aplicación clínica en la medicina regenerativa
Dra. Vianed Marsán-Súarez,I Dra. Miriam-Sánchez Segura,I Dra.C.M. Consuelo Macías-AbrahamI
RESUMEN
Se describen los aspectos más relevantes de las células madre mesenquimales que incluyen su plasticidad hacia diversos linajes celulares, como condrocitos, osteocitos y adipositos, entre otros. Dichas células se pueden obtener principalmente de médula ósea, sangre de cordón umbilical y tejido adiposo, de donde se han logrado establecer cultivos que permiten estudiar sus propiedades funcionales y fenotípicas. Estas expresan antígenos CD73, CD90 y CD105 en ausencia de antígenos hematopoyéticos CD34 y CD45, así como diferentes receptores para citocinas y moléculas de adhesión. Futuras investigaciones permitirán conocer diversos aspectos biológicos de estas células, de importancia en su utilización en la medicina regenerativa como medida terapéutica para solucionar una amplia variedad de enfermedades.
INTRODUCCIÓN
Las células madre mesenquimales (CMM) son células adultas multipotentes, con morfología fibroblastoide y plasticidad hacia diversos linajes celulares como condrocitos, osteocitos y adipocitos, entre otros. Estas pueden ser aisladas y expandidas en medio de cultivo debido a sus propiedades de adhesión al plástico, diferenciación y proliferación in vitro.1-10
Las CMM se caracterizan por presentar una morfología en forma de huso con núcleo alargado, central, que contienen de 2 a 3 nucleolos. En estudios de citometría de flujo se han descrito tres subpoblaciones de estas células. Una de células pequeñas, fusiformes y agranulares a las que denominaron RS-1; otra de células pequeñas y agranulares nombrada RS-2; y la última, conformada por células grandes y granulares a las que denominaron células mesenquimales maduras o CMMm. También se ha reportado la presencia de 2 tipos morfológicos en los cultivos, uno con forma fibroblastoide, que es el predominante, y otro representado por células de mayor tamaño y forma romboide.1,11-16
Las CMM pueden ser aisladas de diferentes fuentes, entre ellas: la médula ósea, la sangre de cordón umbilical, tejido adiposo, páncreas, hígado, músculo esquelético, dermis, membrana sinovial y pulpa dental. Varios grupos de investigaciones publicadas han señalado la posibilidad de obtener también estas células de otras fuentes alternativas, como el líquido amniótico y la gelatina de Wharton del cordón umbilical. No obstante, los tejidos más empleados son la médula ósea, la sangre del cordón umbilical y el tejido adiposo.
Estudios recientes han señalado que no existen
diferencias morfológicas ni inmunofenotípicas entre las células obtenidas de estos tejidos, pero los resultados indicaron que aunque la sangre de cordón umbilical tiene un mayor potencial de expansión, su potencial de diferenciación es menor, al no hacerlo hacia un linaje adipogénico.13-17
CARACTERÍSTICAS DE LAS CMM
En cuanto al aislamiento y cultivo a partir de tejido adiposo, las células obtenidas tienen una morfología, fenotipo y capacidad de diferenciación similar a la médula ósea pero con mayor potencial de proliferación. La obtención de muestras de este tejido es poco invasiva y puede hacerse a través de procedimientos como liposucción o abdominoplastia.13,15 (tabla 1).
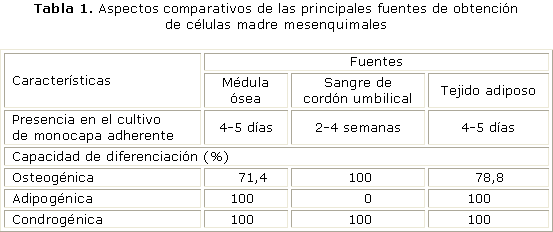
Para que las CMM se puedan clasificar como tales deben expresar los antígenos mesenquimales CD73, CD90 y CD105 y no tener antígenos hematopoyéticos como CD34, CD45, CD14 y CD11b. Además, se ha planteado que las CMM pueden expresar los siguientes antígenos: CD13, CD29, CD44, CD116 y el receptor a del factor de crecimiento derivado de las plaquetas.
Por otro lado, se ha comprobado que las CMM son positivas para otros factores de crecimiento y de matriz celular como: el receptor del factor de crecimiento neuronal, los receptores de factores de necrosis tumoral I y II y los receptores de las interleucinas 1(CD121), 3(CD123), 4(CD124), 6(CD126) y 7(CD127). Expresan diferentes moléculas de adhesión: ICAM-1 (CD54), ICAM-2 (CD102), ICAM-3 (CD50), VCAM (CD106), L selectina (CD62L), LFA-3 (CD58), ALCAM (CD66), NCAM (CD56), endoglobina (CD 105) y CD 72. Por otro lado, estas células son negativas a las reacciones citoquímicas: fosfatasa alcalina, fosfatasa ácida y negro sudán.3,14-20
Existen moléculas de gran relevancia en la hematopoyesis que son producidas y secretadas por las CMM. Estas moléculas incluyen componentes de la matriz extracelular como los colágenos I, III, IV y VI, fibronectina, entre otras; y citocinas que incluyen la interleucina 6 (IL-6), el factor inhibitorio de leucemia, el factor estimulante de colonias de macrófagos, el factor de crecimiento de fibroblastos 1 (FGF-1) y 2 (FGF-2), el factor de crecimiento vascular endotelial (VEGF), etcétera.17,18
CMM Y SUS EFECTOS INMUNOMODULADORES
Debido a la capacidad inmunomoduladora que poseen estas células, pueden evitar el rechazo alogénico mediante diferentes mecanismos. Numerosos estudios han demostrado que las CMM no permiten el reconocimiento de antígenos al interferir en la función de las células dendríticas y de los linfocitos T, por lo que tienen un efecto inmunosupresor local debido a su capacidad de secretar citocinas. Este efecto se potencia cuando las células son expuestas a un medio con actividad inflamatoria o caracterizada por la presencia de altos niveles de interferón gamma.19,21,22
En estudios in vitro se ha demostrado que las CMM no expresan los antígenos del sistema principal de histocompatibilidad de clase II, lo que indica que constituyen un potencial terapéutico en la enfermedad injerto contra huésped porque pueden reducir o suprimir las reacciones inmunes inducidas.19,23,24
Además, pueden afectar el funcionamiento del sistema inmune por otros mecanismos. Se ha indicado que las CMM pueden inhibir la proliferación de linfocitos inducida por aloantígenos y mitógenos como fitohemaglutinina y concavalina A, así como su activación por anticuerpos anti CD3 y CD28. También se ha señalado que las CMM pueden inhibir la expresión de moléculas involucradas en la presentación de antígenos y en cocultivo con células mononucleares de sangre periférica, incrementan la proporción de subpoblaciones de linfocitos T con fenotipo de células reguladoras.25,26
Se ha sugerido que muchos de estos efectos son mediados predominantemente por factores paracrinos, pues las CMM secretan un número considerable de factores inmunomoduladores. También se ha planteado que la acción inmunosupresora pudiera estar vinculada con la participación de otros sistemas inmunorregulatorios.
Como complemento de los datos antes expuestos, se puede acotar que las CMM in vitro pueden inhibir la proliferación de los linfocitos T y B, apoyan el desarrollo de células T reguladoras, disminuyen la actividad lítica de las células citotóxicas naturales o asesinas naturales (en inglés, natural killer cells) y de los linfocitos T citotóxicos, inhiben la diferenciación de monocitos en células dendríticas.27
APLICACIONES CLÍNICAS DE LAS CMM
Debido a la gran capacidad multipotencial, plasticidad y acciones de las CMM, resultan de gran interés para la aplicación clínica (tabla 2). Sus características permiten utilizarlas para modular reacciones inmunes en enfermedades autoinmunes y en el trasplante de médula ósea; para regenerar tejidos destruidos o dañados como sucede en enfermedades neurodegenerativas, la diabetes o en cardiopatías. Además, podrían ser utilizadas como vehículo terapéutico de genes; como por ejemplo, en enfermedades monogénicas como la hemofilia.19,20

El uso clínico de las CMM está basado en una serie de investigaciones preclínicas en modelos animales, que han demostrado la utilidad de estas células en la regeneración de órganos y tejidos, y además se ha observado que modulan reacciones inmunes en distintas enfermedades.19-22
En la reparación del miocardio se reportan diferentes efectos de las CMM sobre el tejido cardíaco, como son su diferenciación in situ en cardiomiocitos, además de la liberación de factores solubles y su fusión con células cardíacas. Esta aplicación se ha demostrado en el corazón porcino donde se ha observado una reducción importante del tamaño del tejido lesionado, neovascularización y reducción de los niveles de apoptosis.21,24
Otra aplicación clínica de las CMM es en la reparación de hueso. Se ha demostrado in vivo en ratones y perros con defectos cráneo-faciales y de los huesos largos, que con la administración directa de estas células y con el uso sobre matrices como la hidroxiapatita/fosfato tricálcico, los resultados son satisfactorios. Recientemente se ha planteado la posibilidad de usar este proceder para optimizar los implantes dentales. En la actualidad, los ensayos clínicos en niños con osteogénesis imperfecta han logrado obtener osteoblastos funcionales que aumentan el contenido mineral del hueso.20,23
En el campo de la oftalmología, la utilización de las CMM empieza a dar sus resultados en el tratamiento de las úlceras corneales y en las degeneraciones retinianas.
Por otro lado, se han obtenido resultados prometedores en el área de la cirugía general en el tratamiento de fístulas de distintas localizaciones como el tracto respiratorio y digestivo. Además, se están realizando importantes estudios en la diabetes mellitus, en enfermedades neurodegenerativas y en la regeneración hepática.1,19,24
Con resultados muy positivos se emplean estas células en quemados, en lesiones cutáneas secundarias a radioterapia, donde se ha demostrado una regeneración epitelial, angiogénesis y una importante hidratación hística. Se están realizando diferentes estudios para la utilización de las CMM en la cicatrización de las heridas, ya sea mediante una administración sistémica o por aplicación tópica en el sitio de la herida. Debido a la naturaleza expuesta de la piel, la aplicación directa de estas células en casos de individuos politraumatizados y en quemaduras graves es una opción muy prometedora. El uso de las CMM en el tratamiento de las heridas crónicas tiene objetivos múltiples: acelerar la reparación del tejido, para amortiguar eventos inflamatorios y para reducir o eliminar la formación de cicatrices.
Otra alternativa es utilizar las CMM para estimular la angiogénesis. Algunos estudios han demostrado que estas células tienen un efecto positivo en la recuperación del flujo sanguíneo, lo cual se explica por la evidencia experimental que indica la generación e incorporación de células endoteliales derivadas de las CMM, a los capilares en su formación y por los resultados de estudios recientes que han demostrado que estas células también promueven la angiogénesis por la secreción de citocinas como VEGF-A, FGF-2 y la IL-6.17,20-

